« La meilleure façon de prédire l’avenir est de le créer »
(Peter Drucker – Professeur, auteur et théoricien)

Chez Macopharma, nous croyons en l’innovation pour atteindre notre objectif d’améliorer les standards en matière de soins. De l’innovation incrémentale à l’innovation radicale et de rupture, nous nous organisons avec des experts pluridisciplinaires : notre comité d’innovation.

Qu’est-ce qu’une innovation ?
Une entité nouvelle ou modifiée qui crée ou redistribue de la valeur (AFNOR, ISO 56000).
Le degré d’innovation peut être exprimé par les attributs d’une innovation (ISO 56000) :
Incremental innovation : progressive changes (ISO 56000)
Gradual, continuous improvements on existing products, services, processes, …
Innovation radicale : changements complétement nouveaux ou significatifs (ISO 56000)
se situe à l’autre bout de la chaîne de valeur par rapport à l’innovation incrémentale
Ex : percée technologique qui transforme les industries – peut créer un nouveau marché
Innovation de rupture : remplace les offres établies (ISO 56000)
En tant que l’un des principaux acteurs de la promotion de la préparation des concentrés plaquettaires, notre mission est de comprendre les besoins des clients et de fournir des solutions pour les aider dans la production de produits qualitatifs et sûrs. Notre observation du processus de préparation des plaquettes nous a conduit à la conclusion que celle-ci est actuellement longue, exigeante et complexe. Afin de compléter son offre et d’optimiser ce processus, Macopharma a donc conçu Maconnect, le tout premier dispositif de connexions stériles multiples.

Sa procédure en une
seule étape permet
jusqu’à
connexions
Le temps nécessaire pour
connecter un pool de
Buffy Coat est inférieur à
secondes
Spécialement conçu pour les opérations de pooling
Maconnect est un concept unique et innovant, spécialement conçu pour optimiser, simplifier et accélérer le processus de préparation des plaquettes, tout en garantissant la préparation d’un concentré plaquettaire sûr.
Maconnect est le tout premier dispositif de connexions stériles multiples, spécialement conçu pour les opérations de pooling.
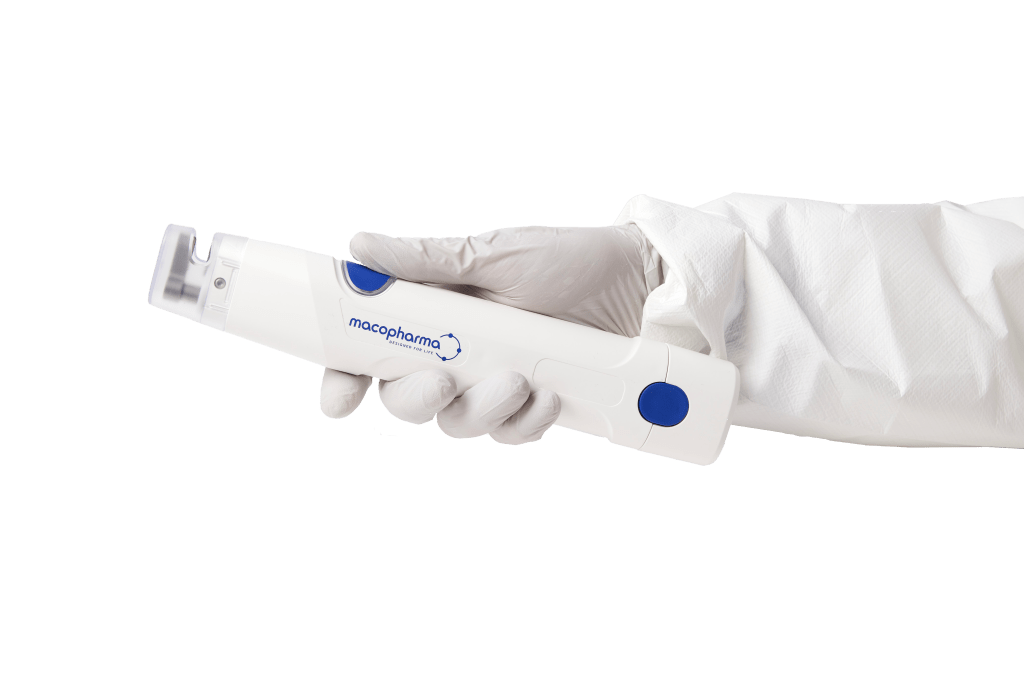
La MacoSeal Light est la nouvelle innovation de Macopharma, une soudeuse sans fil dotée d’une grande autonomie de batterie, d’une forme compacte et légère unique ainsi que d’un bouton de soudure intuitif exceptionnel permettant toutes les configurations d’utilisation.
Le design remarquable de la MacoSeal Light a été conçu pour augmenter les capacités de l’appareil tout en optimisant son ergonomie et en réduisant les efforts manuels.
Poids
Charge complète
de la batterie
Soudures par charge
de batterie


Pas de compromis :
Macopharma bannit le DEHP, pour garantir des solutions de composants sanguins
SÛRES et SÉCURISÉES à tous les patients à travers le monde !
Plus que des mots, nous nous engageons à agir et à respecter notre mission :
We support life !
nous considérons le passage au
sans DEHP comme une INNOVATION.
Parce que la valeur des futurs systèmes de poches est liée à la sécurité, nous avons dédié une équipe complète d’experts scientifiques à la recherche, au design et au développement de nos nouveaux kits en tant qu’INNOVATION pure.
Moindre fuite par rapport au DEHP5-7
Risques liés à l’environnement moindres
(1) Wirnitzer U, Rickenbacher U, Katerkamp A, Schachtrupp A. Systemic toxicity of di-2-ethylhexyl terephthalate (DEHT) in rodents following four weeks of intravenous exposure. Toxicology Letters 2011; 205 (1): 8-14.
(2) Carlson KR. U.S. Consumer Product Safety Commission (CPSC). Toxicity Review for Di-2-ethylhexyl Terephthalate (DEHT). Risk Science Center Department of Environmental Health, University of Cincinnati, 2018.
(3) SCENIHR (Scientific Committee on Emerging and Newly-Identified Health Risks), Scientific Opinion on the safety of medical devices containing DEHP-plasticized PVC or other plasticizers on neonates and other groups possibly at risk. 2015.
(4) Kambia N, Séverin I, Farce A, Dahbi L, Dine T, Moreau E, Sautou V, Chagnon MC. Comparative Effects of Di-(2-ethylhexyl)phthalate andDi-(2-ethylhexyl) terephthalate Metabolites on Thyroid Receptors: In Vitro and In Silico Studies. Metabolites 2021; 11:94.
(5) Graminske S, Puca K, Schmidt A, Brooks S, Boerner A, Heldke S, de Arruda Indig M, Brucks M, Kossor D. In vitro evaluation of di(2-ethylhexyl)terephthalate-plasticized polyvinyl chloride blood bags for red blood cell storage in AS-1 and PAGGSM additive solutions. Transfusion 2018; 58:1100-1107
(6) Nielsen BS, Andersen DN, Giovalle E, Bjergstrøm M, Larsen PB. Alternatives to classified phthalates in medical devices. Dan. Minist. Environ. 2014.
(7) Thelliez et al. Migration of di(2-ethylhexyl) phthalate, diisononylcyclohexane-1,2-dicarboxylate and di(2-ethylhexyl) terephthalate from transfusion medical devices in labile blood products: A comparative study. Vox Sang 2023; 118(7):533-542.
* Phosphate-Adenine-Glucose-Guanosine-Saline-Mannitol
** Saline-Adenine-Glucose-Mannitol
L’usage de la solution PAGGSM dans les kits DEHT diminue l’hémolyse des globules rouges et en améliore la qualité1,2
La solution PAGGSM est utilisée depuis plusieurs décennies en Allemagne et a contribué à accroitre la durée de conservation de 42 à 49 jours3,4
Aucun impact sur l’efficacité clinique et la sécurité des patients n’a été reporté (Allemagne, Suisse)
(1) Larsson L, Sandgren P, Ohlsson S, Derving J, Friis-Christensen T, Daggert F, Frizi N, Reichenberg S, Chatellier S, Diedrich B, Antovic JP, Larsson S, Uhlin M. Non-phthalate plasticizer DEHT preserves adequate blood component quality during storage in PVC blood bags. Vox Sang 2021; 116:60–70.
(2) Graminske S, Puca K, Schmidt A, Brooks S, Boerner A, Heldke S, de Arruda Indig M, Brucks M, Kossor D. In vitro evaluation of di(2-ethylhexyl)terephthalate-plasticized polyvinyl chloride blood bags for red blood cell storage in AS-1 and PAGGSM additive solutions. Transfusion 2018; 58:1100-1107
(3) Hess J. Extended Liquid Storage of Red Blood Cells. In: Blood Donors and the Supply of Blood and Blood Products. Manning FJ, Sparacino L, Eds. Washington DC: The National Academies Press, 1996.
(4) Flegel WA, Natanson C, Klein HG. Does prolonged storage of red blood cells cause harm? Br J Haematol 2014; 165:3-16.
Etude EFS / SFS
(1) Wirnitzer U, Rickenbacher U, Katerkamp A, Schachtrupp A. Systemic toxicity of di-2-ethylhexyl terephthalate (DEHT) in rodents following four weeks of intravenous exposure. Toxicology Letters 2011; 205 (1): 8-14.
(2) Carlson KR. U.S. Consumer Product Safety Commission (CPSC). Toxicity Review for Di-2-ethylhexyl Terephthalate (DEHT). Risk Science Center Department of Environmental Health, University of Cincinnati, 2018.
(3) SCENIHR (Scientific Committee on Emerging and Newly-Identified Health Risks), Scientific Opinion on the safety of medical devices containing DEHP-plasticized PVC or other plasticizers on neonates and other groups possibly at risk. 2015.
(4) Kambia N, Séverin I, Farce A, Dahbi L, Dine T, Moreau E, Sautou V, Chagnon MC. Comparative Effects of Di-(2-ethylhexyl)phthalate andDi-(2-ethylhexyl) terephthalate Metabolites on Thyroid Receptors: In Vitro and In Silico Studies. Metabolites 2021; 11:94.
Etude CBS/NETCAD
Les concentrés de globules rouges dérivés du sang total, prélevés et conservés dans les prototypes de kits de collectes DEHT/PAGGSM, présentent une qualité acceptable jusqu’à leur expiration à 42 jours.
Dans l’ensemble, la qualité in vitro des concentrés de globules rouges “chauds” dans le DEHT/PAGGSM a indiqué :
Changements de déformabilité observés au niveau de la membrane des globules rouges, probablement liés à l’absence de DEHP.
Walsh GM, Howell A, Stephenson T, Olafson C, Blake J, Sumian C, Reichenberg S, Brebant Q, McTaggart K. AABB 2024, P-BC-38.


réalisées avec